Cáncer de Próstata
- El cáncer de próstata es la primera neoplasia maligna en varones, sin considerar los cánceres dermatológicos. Es la tercera causa de muerte de origen oncológico. (1).
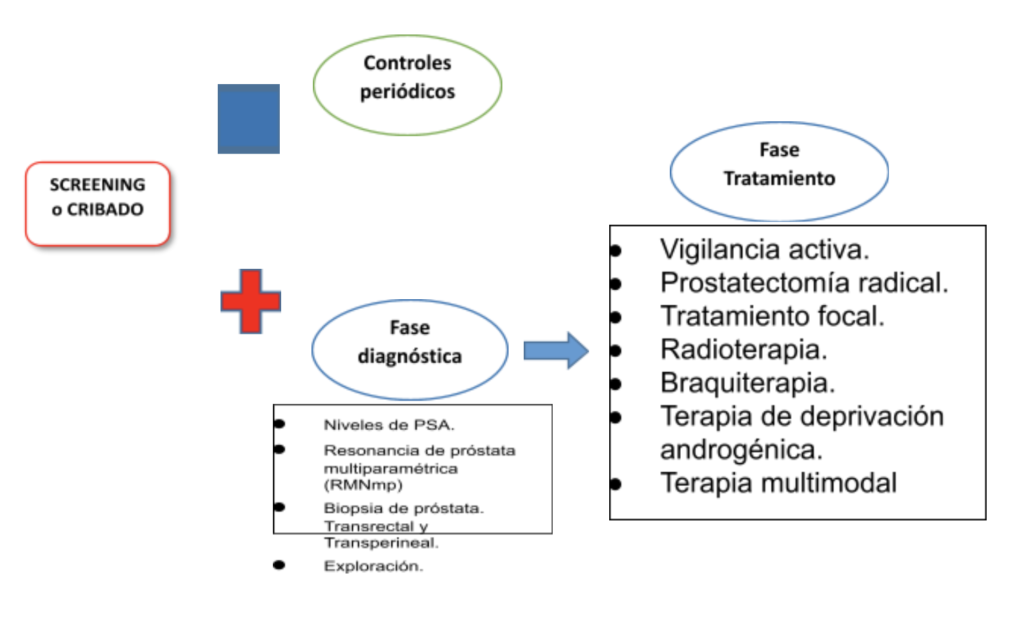

FASE SCREENING; PREGUNTAS MÁS FRECUENTES

Si el tacto rectal y/o los niveles de PSA están alterados el paciente pasará a la fase diagnóstica.
EL PSA o antígeno prostático específico es un marcador específico de órgano (se produce en la próstata) pero no de esta enfermedad (cáncer de próstata), por lo que puede elevarse en patología prostática no neoplásica, en general se dice que los valores normales son hasta 4ng/ml, pero esto es un valor orientativo puesto que hasta el 25% de los cánceres de próstata tienen niveles de PSA inferiores. Por lo que es importante ajustar los niveles de PSA a la edad del paciente y al tamaño de la próstata. En general podemos decir que para pacientes jóvenes lo ideal es un PSA por debajo de 3 ng/ml. (2 y 4). Estas cifras no son válidas en pacientes con cáncer de próstata familiar o hereditario donde el riesgo de padecerlo es mayor.
Cociente PSA libre/PSA total (cociente < 20-25% ayuda a indicar la biopsia prostática en pacientes con PSA 3-10 ng/ml y tacto rectal negativo). También la densidad de PSA (valor del PSA dividido volumen prostático) ayuda a optimizar la decisión de biopsiar o no. En casos dudosos, existen biomarcadores en sangre y orina más precisos que el PSA para la decisión de biopsiar, pues dan una predicción de riesgo de cáncer de próstata significativo, así como la información que nos proporciona la resonancia magnética prostática (ver más adelante).
Los pacientes con dutasterida o finasteride inhibidores de la enzima 5-alfa reductasa medicación usada para mejorar la micción por síntomas prostáticos y también para reducir la caída de cabello, produce una falsa reducción de los niveles del PSA en aproximadamente 50%. Es decir, si yo uso esta medicación y en la analítica me sale un PSA 1.5ng/ml hay que multiplicar este valor por 2 para obtener el valor real en este caso sería de 3ng/ml. De no tener en cuenta esto se pude retrasar el diagnóstico pensado erróneamente que uno tiene niveles normales de PSA. (2, 3 y 4).
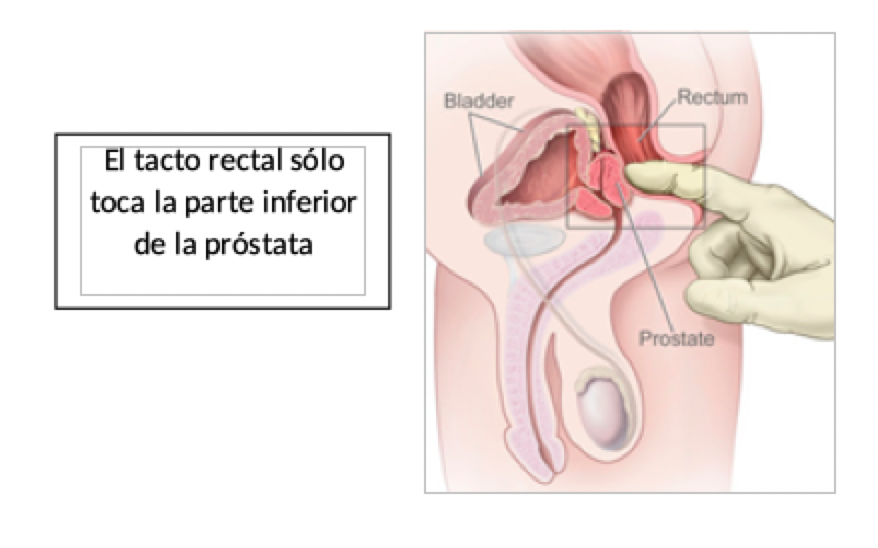
Take-home message. (Importante):
El Tacto rectal, teniendo en cuenta cada caso en manos expertas puede llegar a tener una especificidad y sensibilidad cercana a 60%. (2).
El PSA es órgano específico NO cáncer específico. La elevación del PSA puede ser por factores no oncológicos: Infecciones de orina, prostatitis, instrumentación de la vía urinaria, etc. Por lo tanto, un PSA alterado debe ser verificado con un 2º análisis separado al menos 2-3 semanas antes de darlo como sospechoso de cáncer. (2).
Factor familiar: si tienes uno o más familiares de primera línea con cáncer de próstata antes de los 65 años y/o si eres portador de gen BCRA2. Aconsejable iniciar el screening a los 40 o 45 años. (2). También en familias con cáncer de mama & ovario o de síndrome de Lynch.
Hay que tener en cuenta el PSA según la edad del paciente, en un paciente menor de 60 años, ideal es tener niveles menores 3ng/ml. (4).
Los síntomas urinarios como levantarse a orinar por las noches, el chorro flojo, el goteo, el pujo, etc. generalmente estás asociado a la patología benigna conocida como hipertrofia de próstata (HBP), pero también pueden estar presentes en el cáncer de próstata. Por síntomas, ambas entidades no son diferenciables.
Dutasterida o finasteride, produce una falsa reducción de los niveles del PSA en aproximadamente 50%. Si no se tiene en cuenta esto a ver los valores de PSA en la analítica se puede creer erróneamente que uno está en niveles de normalidad.
FASE DIAGNÓSTICA; PREGUNTAS MÁS FRECUENTES:
La única forma de diagnosticar en forma definitiva el cáncer de próstata es mediante biopsia de próstata.

El adenocarcinoma prostático es una lesión multifocal en el 78% de los casos. El 60-70 % de los cánceres se originan en zona periférica, el 10-20% en la zona transicional y el 5-10% en la zona central. (2 y 3).
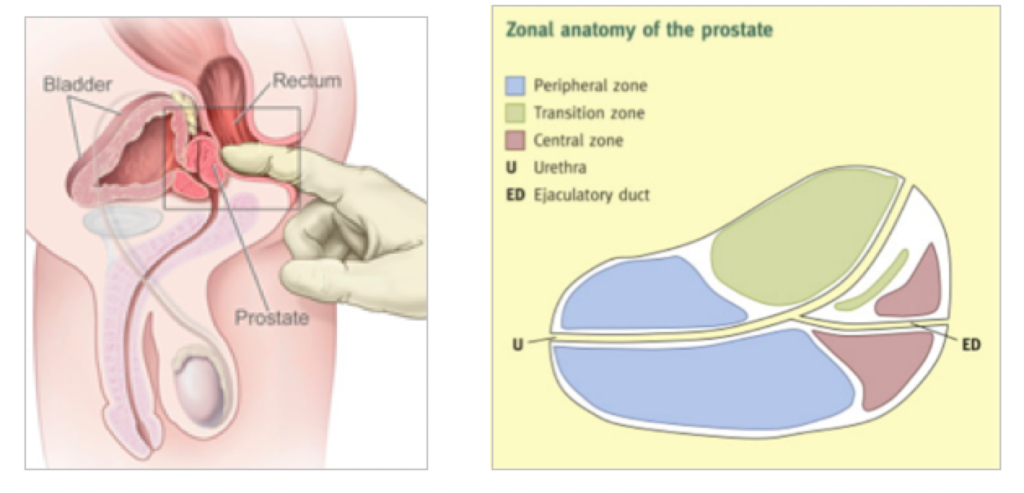
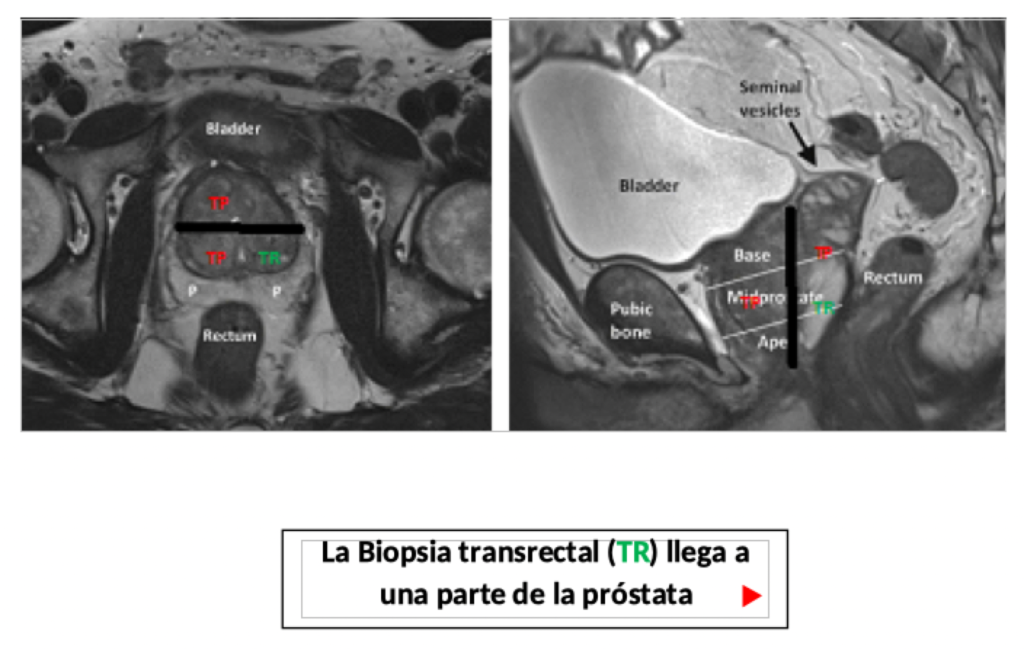
Como pueden ver en la figura, con el tacto rectal se puede alcanzar sólo una parte de la zona periférica de la próstata y por lo mismo la biopsia transrectal sólo llega a una parte de la próstata. Por ello, cuando se repiten una o más biopsias por vía transrectal, ello no exime de que pueda existir un cáncer de próstata en la parte anterior de la próstata. (3).
Imagínese tener un cáncer en la parte superior o en la zona central (llamada transicional), es factible la posibilidad de no diagnosticarlo con una biopsia transrectal.
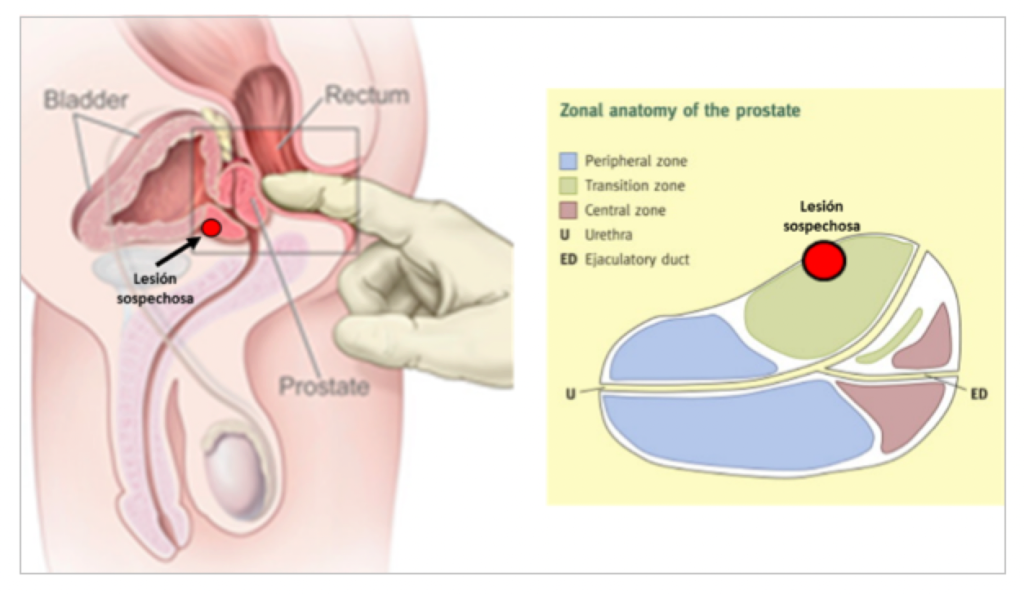
Nosotros aconsejamos no hacer biopsias a ciegas como se han venido haciendo durante muchos años. Es recomendable el uso de la resonancia de próstata multiparamétrica (RMmp) previa a la biopsia, la cual nos va a permitir encontrar y ubicar la zona sospechosa de cáncer de próstata. Según la ubicación y las características de la próstata podremos escoger el abordaje de la biopsia. Incluso en casos dudosos para biopsia, una RMmp que no ve lesiones sospechosas pueda obviar la necesidad de biopsia.
Primero una resonancia de próstata multiparamétrica.
Nos ayuda junto con la exploración y el PSA a tomar la decisión de biopsiar la próstata.
Nos da información si hay alguna lesión, la probabilidad de malignidad, las características y su ubicación.
La ubicación es importante para escoger el tipo de biopsia.
En paciente con biopsia transrectal previa, pero con PSA alterado, la resonancia nos permite ver si existe alguna lesión sospechosa en alguna zona no accesible a la vía transrectal.
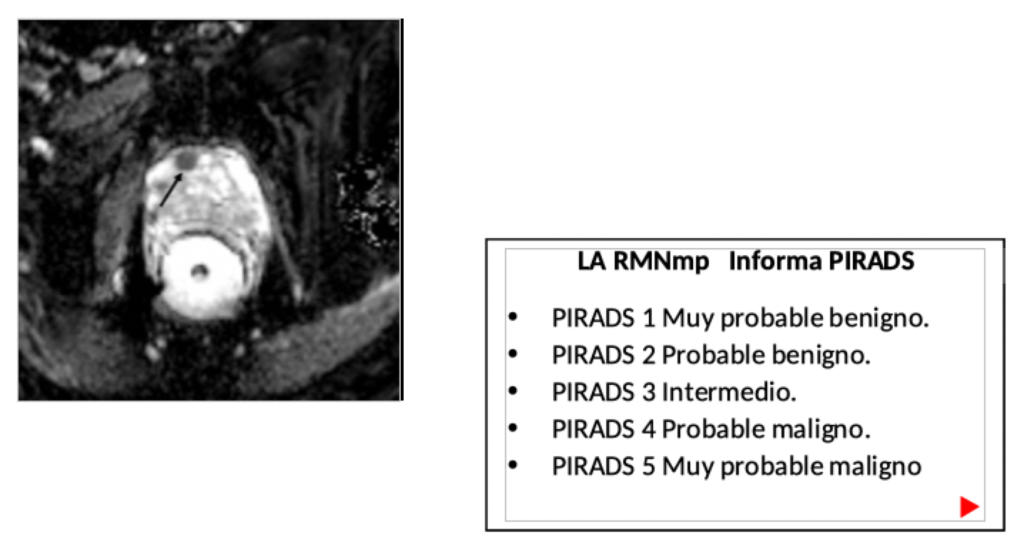
Tipos de biopsia de próstata.
Biopsia de próstata transrectal con guía ecográfica. Es la biopsia clásica, que se basa en la obtención de 12 u 14 cilindros, de la zona periférica prostática (El 60-70 % de los Cánceres se originan en zona periférica, el 10-20% en la zona transicional y el 5-10% en la zona central). El inconveniente principal es que se llega de manera subóptima a las zonas anterior y central, sobre todo en próstatas de más de 50-60cc. Además, si solo se ha hecho ecografía transrectal, las imágenes ecográficas convencionales no son capaces de detectar de manera efectiva las zonas sospechosas. (2 y 3).
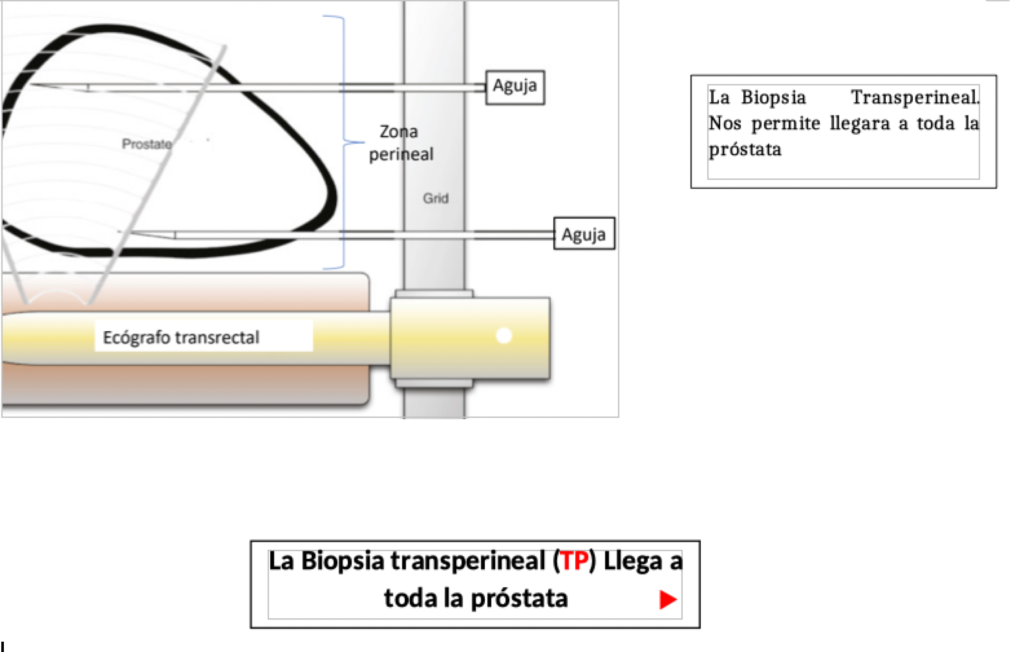
Biopsias de Próstata Fusión transperineal
Recomendable para pacientes con biopsia o biopsias de próstata transrectal previas en los cuales persiste la sospecha de cáncer de próstata o en pacientes con lesiones no asumibles vía transrectal por su ubicación referida por RMmp). Esta hace un mapeo completo e íntegro de la próstata, detallando si existe zonas compatibles con cáncer de próstata significativo, El sistema fusión, se basa en que, si la RMmp ha detectado zonas PIRADS 4 y/o 5, y en algunos casos 3, en el momento de la biopsia dichas imágenes sospechosas, en tiempo real, se fusionan con el ecógrafo, dándonos una precisión para la obtención de la muestra. El abordaje transrectal o transperineal se decide en base a las imágenes obtenidas en la resonancia, la cual nos permite valorar la accesibilidad de la zona sospechosa. Mediante este sistema se puede abarcar cualquier zona de la próstata, además de permitimos valorar si la enfermedad está localizada en el órgano o no. (2 y 3).
La segunda ventaja de la biopsia transperineal frente a la transrectal es que produce menos infecciones al evitar la flora rectal. El incoveniente es que generalmente requiere sedación o anestesia epidural porque el número de biopsias es mayor, lo que también conlleva un riesgo algo mayor de retención urinaria posterior, que se resuelve en 2-3 días cuando ocurre (aprox 5%). La última ventaja de la biopsia mapeo transperineal + biopsias de fusión es que la caracterización prostática es mucho mejor y ello es obligatorio si se opta por las estrategias conservadoras como vigilancia activa o tratamiento focal.
Take-home message. (importante):
La única forma de diagnosticar en forma definitiva el cáncer de próstata es mediante biopsia de próstata.
La decisión de biopsiar la próstata es conjunta con el paciente, basada en la historia clínica, la exploración, pruebas complementarias (PSA, RMN, marcadores, etc.) y no sólo por un nivel de PSA.
Sobre la base a si existen o no zonas sospechosas de cáncer de próstata además de la ubicación y características, en conjunto con el paciente se toma la decisión de realizar una biopsia y la vía por donde acceder a la próstata. Así evitamos tener que someter a los pacientes a biopsias a ciegas vía transrrectal.
Si se sigue sospechando de un cáncer de próstata y tienes una o varias biopsias transrectal, no es aconsejable seguir haciendo biopsias por vía transrectal.
Se puede afinar con una resonancia de próstata multiparamétrica para valorar la posibilidad de biopsia transperineal +/- fusión según hallazgos.
FASE TRATAMIENTO; PREGUNTAS MÁS FRECUENTES:

Decir que uno tiene cáncer de próstata no es suficiente. Tenemos que saber su características y si está sólo en la próstata o también por fuera de ella (locamente avanzado, solo en la pelvis o también a distancia con metástasis. Para esto nos valemos de una clasificación clínica (PSA, exploraciones y pruebas complementarias) y patológica (biopsia).
Pues una vez diagnosticado con biopsia tenemos que asignarle un grupo de riesgo (NCCN.org).
El ubicarnos en grupo de riesgo, nos orienta a cosas como: a mayor riesgo hay mayor posibilidad de que el cáncer esté también por fuera de la próstata y por ende más agresivo. Ejemplo un riesgo alto implica que debamos pedir pruebas complementarias como TAC y gammagrafía ósea (llamados estudios de extensión) para descartar si hay afectación de otros órganos. También es importante para la elección del tratamiento, pues por ejemplo en un cáncer de próstata de bajo riesgo es aconsejable una prostatectomía radical, pero si se tratase de un cáncer de próstata alto riesgo además se recomienda linfadenectomía pélvica.
El siguiente cuadro es orientativo, puesto que un tratamiento siempre tiene que ser individualizado. (2, 3 y 6).
Grupos de Riesgo | Características | Opciones de tratamiento. Recomendaciones +++/++/+ |
Muy bajo riesgo | Biopsia G3+3 hasta 3 muestras positivas y PSA <10ng/ml y Tacto rectal normal. | Vigilancia Activa +++. Observación ++. Prostatectomía sin linfadenectomía +. Tratamiento focal +. Braquiterapia +. |
Bajo riesgo | Biopsia G3+3 y PSA <10ng/ml y Tacto rectal normal o algún nódulo palpable en un lado de la próstata. | Prostatectomía sin linfadenectomía +++. Terapia Focal ++ Vigilancia Activa ++ Braquiterapia + Radioterapia sin TDA + |
Riesgo intermedio Si cumple al menos 2 características. | Favorable intermedio. Biopsia G3+4 PSA 10ng/ml – 20 ng/ml Tacto rectal alterado en un o los dos lados de la próstata Desfavorable Intermedio. Biopsia G4+3 PSA 10ng/ml – 20 ng/ml Tacto rectal alterado en un o los dos lados de la próstata. Se debe pedir estudio de extensión Antes de ofrecer tratamiento, se debe pedir: TAC y gammagrafía ósea, para saber si el cáncer afecta también está fuera de la próstata. | Prostatectomía C/S linfadenectomía +++. Braquiterapia ++. Radioterapia con TDA ++. Terapia Focal +. Terapia multimodal +. Prostatectomía con linfadenectomía +++. Radioterapia con TDA ++ Braquiterapia +. Terapia multimodal +++. |
Alto riesgo Si cumple al menos 2 características. | Biopsia G4+4, G3+5 o G 5+3 PSA > 20 ng/ml Tacto rectal alterado impresiona fuera de la próstata. Antes de ofrecer tratamiento, se debe pedir: TAC y gammagrafía ósea, para saber si el cáncer afecta también está fuera de la próstata. | Prostatectomía con linfadenectomía +++. Radioterapia con TDA+++. Terapia multimodal +++. |
Muy alto riesgo | Biopsia G4+5, G5+4 o G 5+5 Tacto rectal alterado impresiona fuera de la próstata. Antes de ofrecer tratamiento, se debe pedir: TAC y gammagrafía ósea, para saber si el cáncer afecta también está fuera de la próstata | Prostatectomía con linfadenectomía +++. Radioterapia con TDA+++. Terapia multimodal +++ |
GMO: gammagrafía ósea. TDA terapia de deprivación androgénica. Linfa: exéresis de linfa pélvica.
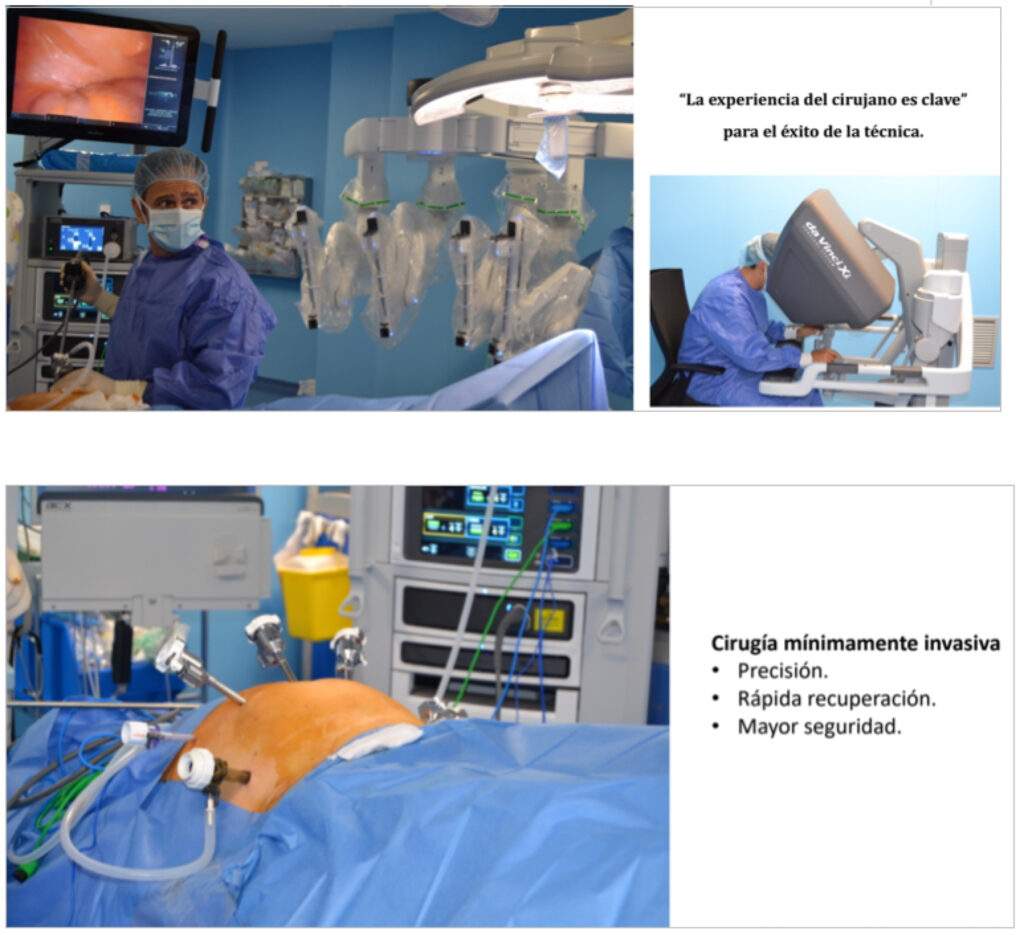
Prostatectomía Radical. Consiste en extirpar la próstata y vesículas seminales, en grupos de riesgo intermedio desfavorable, alto y muy alto es necesario la exéresis de los ganglios linfáticos; es la técnica de referencia para el manejo de cánceres localizados y localmente avanzados, consiguiendo un porcentaje de curación superior al 90 % y una supervivencia libre de enfermedad superior al 95%. Existen 3 abordajes con resultados oncológicos similares en un cirujano experimentado: Abierto y mínimamente invasivo (laparoscópico y robótico). A favor del abordaje mínimamente invasivo, tenemos una menor estancia hospitalaria, menor dolor, una recuperación más rápida, una menor tasa de transfusiones, lo que permite al paciente reintegrase a su actividad habitual con mayor prontitud. La cirugía robótica nos permite mejorar la preservación de nervios y vascularización responsables de la erección cuando ello es posible, realizar mejor la preservación del mecanismo esfinteriano y la unión entre vejiga y uretra (anastomosis), redundando en mejores tasas de continencia postoperatoria dependiendo siempre de la experiencia del cirujano (7 y 8).
Por encima del 90% de pacientes recuperan la continencia urinaria en un periodo no mayor de un año; para acortar ese periodo de recuperación nuestros pacientes siguen un programa de rehabilitación de suelo pélvico antes y después de la cirugía. (2 y 3).
La incontinencia urinaria, en caso de que el paciente no responda al programa de rehabilitación del suelo pélvico, se puede solventar quirúrgicamente. Del mismo modo el uso de inhibidores de la fosfodiesterasa tipo 5 es clave para la recuperación de la función sexual, en casos severos se puede solucionar quirúrgicamente. (5).
Vigilancia activa. Es una alternativa para los cánceres de próstata de muy bajo y bajo riesgo que en general no crean ningún problema clínico ni de supervivencia. El objetivo es reducir el sobre tratamiento minimizando los efectos secundarios, relacionados con el tratamiento, sin comprometer la supervivencia. Pero hay que seguir unos criterios muy exigentes de selección y aceptar un protocolo de seguimiento estricto que le tendremos que explicar de forma detallada, dado que aproximadamente un 30-50% de los pacientes requerirán tratamiento activo a los 10 años de seguimiento.
Vigilancia activa. | |
Intención de tratamiento. | Curativo cuando progrese |
Seguimiento. | PSA semestral, tacto anual y RMNmp + biopsia cada 3 años |
Objetivo | Minimizar los posibles efectos secundarios del tratamiento activo |
A quien va dirigido | Muy bajo riesgo y bajo riesgo. |
Tratamiento activo | Si hay progresión de enfermedad y/o si el paciente lo solicita. |
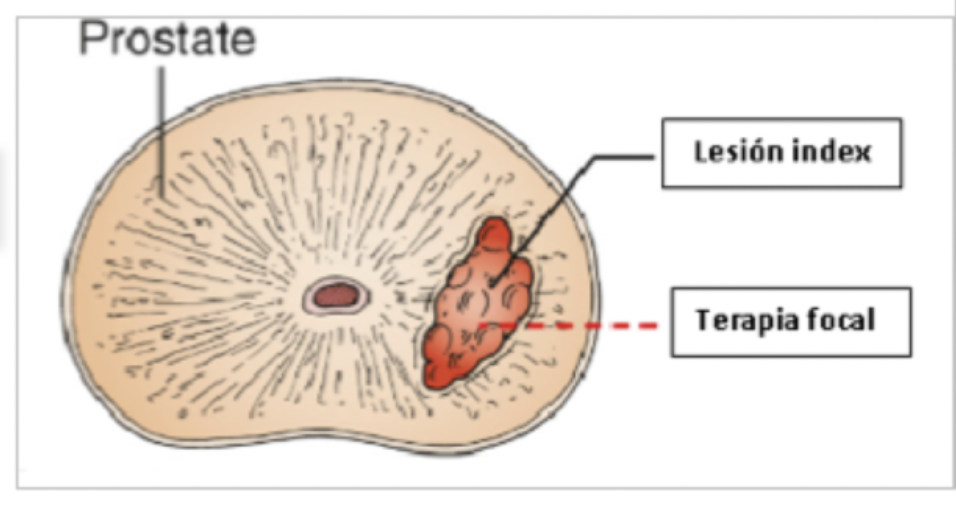
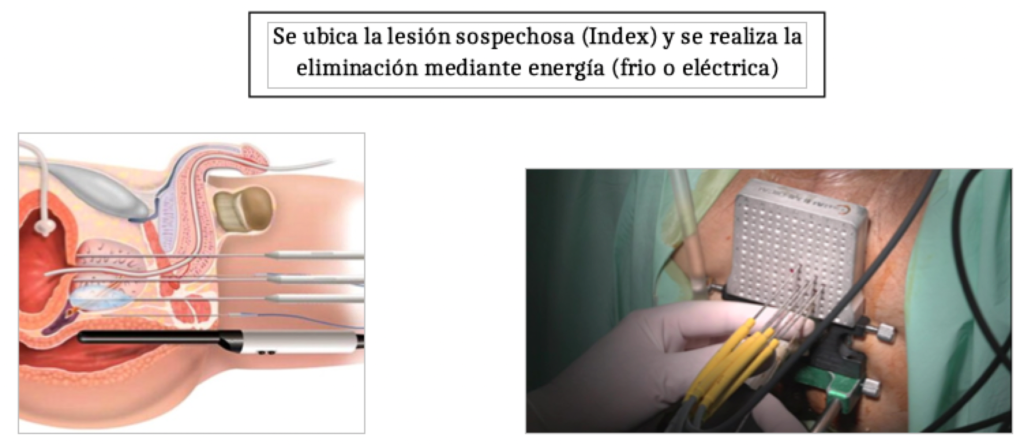
Terapia focal. Es una alternativa mínimamente invasiva para el cáncer localizado de bajo riesgo y algunos casos de riesgo intermedio. Consiste en la ablación selectiva del cáncer significativo exclusivamente con energías que tratan exclusivamente la zona enferma, reduciendo los efectos secundarios de otras terapias radicales. Como pueden quedar micro focos satélites que no representan riesgo vital para el paciente (cáncer insignificante), si en los controles posteriores requieren de tratamiento se pude brindar una nueva sesión o dar un tratamiento radical. Se usan energía como crioterapia o electroporación irreversible (IRE) o ultrasonidos de alta intensidad (HIFU).
Radioterapia.
Es una opción al manejo del cáncer de próstata, especialmente en pacientes que por sus circunstancias actuales presentan un alto riesgo quirúrgico. Entre las diferentes opciones disponibles, encontramos la radioterapia tridimensional conformada (RT-3D), radioterapia de intensidad modulada (IMRT) y la radioterapia guiada por imágenes (IGRT). Este tratamiento, para obtener mejores resultados oncológicos puede ir acompañado de terapia de supresión androgénica (castración médica) entre 6 a 36 meses, según el estadio de la enfermedad, que suele ser reversible cuando se detiene. (3).
Al igual que la Braquiterapia, puede empeorar los síntomas urinarios, dar molestias al defecar, hematuria, sangrado digestivo etc.
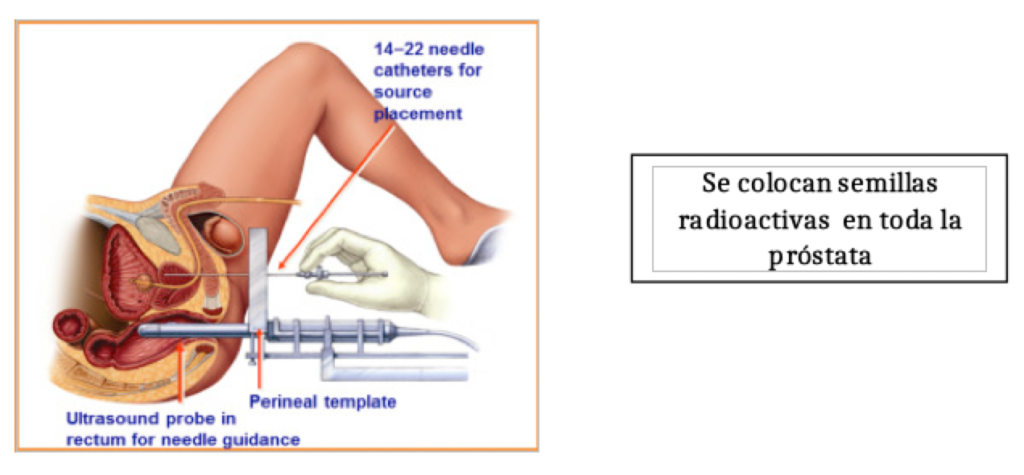
Braquiterapia. Colocación en la próstata vía transperineal de semillas radiactivas permanentes, nuevamente dependiendo del grado (Importante una biopsia precisa y de calidad) puede que tenga que ser asociado o no a radioterapia externa. (3).
Terapia multimodal.
Basados en que el cáncer es dependiente de la hormona masculina, la testosterona, su bloqueo mediante tratamiento hormonal (castración médica) permite detener su crecimiento, aunque este efecto es temporal (no definitivo), porque el tumor finalmente se hará resistente a la castración. El tratamiento hormonal está destinado a los pacientes con cáncer de próstata avanzado o metastásico o en progresión a tratamientos locales. En estos casos, hay que individualizar a cada paciente y las alternativas de tratamiento se han incrementado exponencialmente en la última década con distintos fármacos que alargan el periodo sin progresión de la enfermedad y la supervivencia global, aportando mejor calidad de vida y el control de los síntomas derivados de la enfermedad cuando progresa a metástasis.
En un futuro inmediato el tratamiento personalizado según la caracterización genética de cada tumor, el tratamiento ablativo dirigido a la enfermedad metastática de baja carga y el unido a radioligandos pueden aún mejorar el pronóstico de muchos pacientes y alargar su supervivencia. Por todo ello, en esta fase de la enfermedad nos apoyamos en equipos multidisciplinares coordinandonos con oncólogos médicos y radioterapeutas, médicos nucleares y genetistas.
Take-home message. (importante):
Basados en un correcto y preciso diagnóstico, el paciente ha de entender sus alternativas, tanto los pro y contras. No siempre un tratamiento activo es la primera opción.
Las opciones de tratamiento deben ser ajustadas a las características de cada tumor y cada paciente.
El saber en qué grupo de riesgo está el paciente, permite orientar sus estudios y proporcionarle qué alternativas terapéuticas tiene, así como pronóstico y seguimiento.
Cuando el cáncer de próstata es metastático o cuando progresa de un tratamiento local con intención curativa, las alternativas de seguimiento y tratamiento son muchas. Cada caso se ha de individualizar y el manejo ha de ser multidisciplinar.
REFERENCIAS.
- Sociedad Española de Oncología médica (SEOM). Las cifras del cáncer en España 2020.
European Association of Urology (EAU). Guideline 2020. Muscle-invasive and Metastatic Bladder Cancer and Primary Urethral Carcinoma.
Partin, Alan W., MD, PhD. Campbell-Walsh-Wein Urology, Twelfth Edition. 2021.
Christian Arsov a, Nikolaus Becker b, Boris A. Hadaschik . Prospective Randomized Evaluation of Risk-adapted Prostate-specific Antigen Screening in Young Men: The PROBASE Trial. European Urology, 2013-12-01, Volume 64, Issue 6, Pages 873-875, Copyright © 2013 European Association of Urology.
Smith, Joseph A., Jr., MD. Hinman’s Atlas of Urologic Surgery, Fourth Edition. 2018.
NCCN Clinical Practice Guidelines in Oncology. 2020.
John W Yaxley, Geoffrey D Coughlin, Suzanne K Chamber. Robot-assisted laparoscopic prostatectomy versus open radical retropubic prostatectomy: early outcomes from a randomised controlled phase 3 study. Lancet, The, 2016-09-10, Volume 388, Issue 10049, Pages 1057-1066, Copyright © 2016 Elsevier Ltd.
Ramsay, C., et al. Systematic review and economic modelling of the relative clinical benefit and cost-effectiveness of laparoscopic surgery and robotic surgery for removal of the prostate in men with localised prostate cancer. Health Technol Assess,
-
HOSPITAL VITHAS 9 DE OCTUBRE DE VALENCIA
Consulta Número 31
Segunda Planta del Edificio de Consultas Externas
Av. Valle de la Ballestera, 59
Teléfono: 963 17 99 31
-
HOSPITAL VITHAS CONSUELO DE VALENCIA
Consulta Número 6
Tercer piso
Teléfono: 963 17 78 00
Horario de atención
-
Lunes a Jueves de 15h a 19h30
Viernes de 9h30 a 13h39 y de 15h a 18h
